Biała czy czerwona?
Poniższy artykuł został opublikowany pierwotnie w czasopiśmie dla nauczycieli Biologia w Szkole (2/2020):

Niewiele jest związków chemicznych tak ważnych dla każdego żywego organizmu jak oksydan, czyli inaczej monotlenek diwodoru H2O, nazywany przez nas częściej po prostu wodą. Woda występuje w w warunkach standardowych w stanie ciekłym. W stanie gazowym wodę określa się mianem pary wodnej, a w stałym stanie skupienia – jak wiadomo - lodem. Dzięki swoim właściwościom chemicznym związek ten w warunkach naturalnych może występować na Ziemi we wszystkich stanach skupienia, co jest właściwie ewenementem.
Woda jest powszechnym rozpuszczalnikiem związków chemicznych o znaczeniu biologicznym. Uczestniczy w przebiegu większości reakcji metabolicznych, stanowi ośrodek transportu wewnątrzustrojowego (m.in. produktów przemiany materii, substancji odżywczych, hormonów i enzymów). Dzięki wysokiej wartości ciepła właściwego i ciepła parowania umożliwia sprawną termoregulację. Wymienione powyżej to tylko niektóre z powodów sprawiających, że omawiana substancja jest nieodzownym uzupełnieniem pokarmu wszystkich znanych organizmów – chociaż ich zapotrzebowanie na nią może być bardzo zróżnicowane. Woda stanowi średnio 70% masy dorosłego człowieka, w tym 60–70% limfy, 95% osocza krwi, 90% liści, owoców, 20% kości, 10% szkliwa zębów, tkanki tłuszczowej.
Jeśli chodzi o rośliny, to wypracowały one pewne mechanizmy związane z gospodarką wodną odmienne niż w przypadku zwierząt. Gospodarkę taką rozumie się jako zespół procesów fizjologicznych, które umożliwiają roślinom utrzymanie właściwej zawartości wody w tkankach. Odpowiednie uwodnienie tkanek jest konieczne w celu zapewnienia ciągłości procesów metabolicznych, transportu ksylemowego i floemowego oraz utrzymania kształtu komórek i całej rośliny. Ciśnienie panujące wewnątrz komórek jest ważnym czynnikiem umożliwiającym wzrost komórek. Jako rozpuszczalnik woda umożliwia transportowanie asymilatów i substancji regulatorowych we floemie oraz soli mineralnych w ksylemie. Parowanie wody z nadziemnych organów roślin umożliwia powstawanie tzw. siły ssącej, która jest siłą napędową transportującą duże masy wody nawet kilkadziesiąt metrów w górę, jak ma to miejsce w przypadku wysokich drzew [1] [2].
W szkolnej, uczelnianej lub nawet hobbystycznej pracowni biologicznej można przeprowadzić wiele doświadczeń związanych z gospodarką wodną różnorodnych organizmów. Przykładem mogą tu być prace ukazujące zasadę zjawiska osmozy przy wykorzystaniu błon biologicznych, a także budowa modelu obrazującego siłę ssącą liści [3] [4]. Innym zjawiskiem związanym z zagadnieniem transportu wody jest plazmoliza, o której wspominałem już dawniej w artykułach. Z korespondencji z Szanownymi Czytelnikami wynika jednak, że pożądane jest, abym poświęcił więcej miejsca samemu zjawisku, jak i metodom jego obserwacji w warunkach podstawowo wyposażonej pracowni.
Doświadczenie
Plazmolizę możemy obserwować w zróżnicowanych komórkach wielu gatunków roślin. Najpowszechniej stosuje się komórki skórki wewnętrznych powierzchni liści spichrzowych cebuli zwyczajnej Allium cepa.
Chociaż wszyscy używamy w odniesieniu do tego znanego wszystkim warzywa określenia "cebula", to prawidłową nazwą botaniczną jest w tym przypadku czosnek cebula. Roślina ta należy do rodziny amarylkowatych Amaryllidaceae - tej samej, w skład której wchodzi wiele roślin ozdobnych, m.in narcyz trąbkowy Narcissus pseudonarcissus [5].
Cebula jest jedną z najdawniej uprawianych przez człowieka roślin i obecnie nie występuje już w stanie dzikim [4]. Roślina pochodzi prawdopodobnie z Azji Środkowej, ale dziś występuje praktycznie na całym świecie. Ślady wskazujące na wykorzystanie cebuli znajdowane są na wykopaliskach w Palestynie pochodzących z epoki brązu, sprzed około 5000 lat p.n.e - są to rysunki przedstawiające to warzywo, a także jego zastosowanie w celach konsumpcyjnych [6].
Cała roślina, a głównie jej cebula jest bogata w przydatne związki chemicze, także w witaminy. Występują w niej olejki lotne, takie jak dwusiarczek alilo-propylowy o charakterystycznym zapachu oraz inne siarczki i związki alkilowe, w tym substancje o silnych właściwościach fitoncydowych, czemu cebula znalazła zastosowanie w medycynie ludowej i fitoterapii [7].
Dzięki prowadzonej przez wieki hodowli otrzymano wiele różnych, tak pod względem wyglądu, jak i smaku oraz wartości odżywczych, odmian. Fotografia 1 przedstawia cebule odmiany białej i czerwonej.
Po przekrojeniu możemy obserwować budowę wewnętrzną tego interesującego organu roślinnego (Fot.2).
Cebula bulbus jest silnie wyspecjalizowanym pędem podziemnym o funkcji spichrzowej i przetrwalnikowej, którego główną część stanowią przekształcone liście. Łodyga rośliny cebulowej jest mocno skrócona i przyjmuje postać tzw. piętki, na której gęsto osadzone są zgrubiałe liście spichrzowe gromadzące substancje zapasowe, przy czym liście zewnętrzne są zwykle martwe i tworzą łuski o funkcji ochronnej. Część nadziemna rośliny bierze swój początek z tak zwanego pąka wierzchołkowego.
Jak widać, obie przedstawione cebule nie różnią się budową, a jedynie kolorem. Okazuje się, że do obserwacji plazmolizy bardziej przydatna jest odmiana czerwona – myślę, że powód takiego stanu rzeczy stanie się za parę chwil jasny.
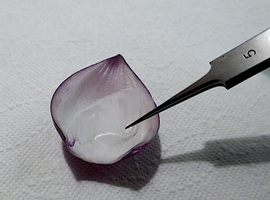
Aby móc obserwować plazmolizę, najlepiej jest naciąć za pomocą skalpela lub żyletki odpowiedni fragment skórki wewnętrznej strony liścia spichrzowego w rejonie oznaczonym na Fot.3 strzałką. Są to rejony szczytowe liścia, po stronie przeciwnej do umiejscowienia piętki cebuli.
Jak widać na Fot.4, w niektórych przypadkach skórka tak łatwo daje się odwarstwić od głębiej leżących warstw komórek, że można ją zdjąć z całej powierzchni liścia właściwie w jednym kawałku. Do doświadczeń polecam pobierać jednak mniejsze fragmenty.
Prawidłowo pobrany fragment skórki ma grubość jednej komórki i powinien szybko zostać umieszczony na szkiełku podstawowym w kropli wody, tak aby nie wysechł, a następnie przykryty szkiełkiem nakrywkowym. Obserwacje prowadzimy w świetle przechodzącym, w jasnym polu.
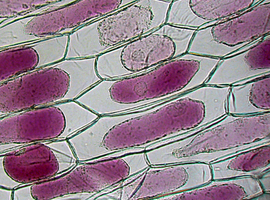
Fotografia 5 pozwala na stwierdzenie, że komórki skórki u obu odmian nie różnią się od siebie kształtem – są wydłużonymi wielokątami. W ich wnętrzu można zauważyć słabo widoczne jądra komórkowe dociśnięte do wewnętrznej powierzchni błony komórkowej poprzez silnie rozrośnięte i zajmujące prawie całą dostępną objętość wakuole (cytoplazma tworzy ledwie dostrzegalną warstwę). Można zauważyć jednak pewną dosyć ciekawą różnicę: protoplast komórek cebuli odmiany białej jest praktycznie bezbarwny, natomiast u odmiany czerwonej ma wyraźne fioletowe zabarwienie spowodowane obecnością barwników antocyjanowych. Takie naturalne wybarwienie sprawia, że obraz komórek odmiany czerwonej cebuli jest dużo bardziej kontrastowy niż w przypadku odmiany białej, co zdecydowanie ułatwia obserwacje mikroskopowe, m.in. w trakcie plazmolizy. Z tego powodu wykorzystanie cebuli odmiany czerwonej jest godne polecenia do wykorzystania w praktyce szkolnej.
Aby zaobserwować plazmolizę badane komórki należy umieścić na kilka, kilkanaście minut np. w dosyć stężonym roztworze glukozy lub sacharozy (roztworze hipertonicznym względem wnętrza komórki), po czym powtórzyć obserwacje. Możemy wtedy zanotować wyraźną zmianę: wakuola wraz z całym protoplastem zmniejsza wyraźnie swoją objętość i zaczyna wyraźnie odstawać od ściany komórkowej (Fot.6).
Różnica stanie się jeszcze bardziej wyraźna, jeśli porównamy Fot.6 z Fot.5B. Plazmolizę możemy odwrócić (o ile w jej trakcie nie zostały zbytnio uszkodzone błony biologiczne komórki) po przeniesieniu preparatu do roztworu hipotonicznego, tj. o mniejszym stężeniu niż we wnętrzu protoplastu.
Wyjaśnienie
Plazmoliza powoduje utratę tzw. turgoru, czyli stanu napięcia ściany komórkowej spowodowanego działaniem ciśnienia hydrostatycznego panującego wewnątrz komórki. Efektem istnienia turgoru jest stan jędrności tkanek roślinnych oraz możliwość zachowania kształtu i sztywności nawet tych elementów, które pozbawione są typowych tkanek mechanicznych.
Osmoza jest zjawiskiem występującym w przypadku, kiedy roztwory o różnym stężeniu zostaną rozdzielone barierą półprzepuszczalną. Bariera posiada tę cechę, że cząsteczki rozpuszczalnika mogą się przez nią przemieszczać bez większych trudności, zaś cząsteczki substancji rozpuszczonej w dużo mniejszym stopniu. Osmoza zachodzi spontanicznie w kierunku od roztworu o niższym stężeniu do roztworu o wyższym, co prowadzi do wyrównania obu stężeń. Efektem tego jest powiększenie się objętości roztworu bardziej stężonego, zmniejszanie zaś mniej stężonego. Jaki jednak mechanizm stoi za tym fenomenem?
Kluczem do zrozumienia osmozy jest fakt istnienia dyfuzji, jako samorzutnego (spontanicznego) procesu rozprzestrzeniania się cząsteczek lub energii w każdym ośrodku o temperaturze wyższej od zera bezwzględnego, co jest spowodowane chaotycznymi zderzeniami cząsteczek budujących rozpatrywany układ. Wprowadzenie do układu bariery półprzepuszczalnej rozdzielającej roztwory o różnym stężeniu pozwala na obserwację interesujących prawidłowości, których zrozumienie powinien pomóc Rys.1.
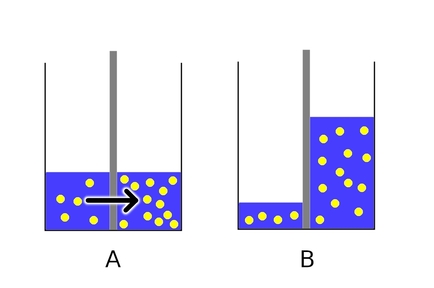
Początkowo (Rys.1.A) po obu stronach bariery półprzepuszczalnej (szara) występują różne stężenia substancji rozpuszczonej (żółte koła) w ten sposób, że w lewej części naczynia stężenie jest mniejsze niż w prawej. Pamiętajmy też, że przez barierę przenikać mogą tylko cząsteczki rozpuszczalnika (niebieski), zaś cząsteczki substancji rozpuszczonej nie posiadają tej zdolności. W takiej sytuacji cząsteczki rozpuszczalnika mają częstszy kontakt z barierą po stronie o niższym stężeniu, ponieważ po przeciwnej stronie istnieje większa ilość cząsteczek substancji rozpuszczonej, jako swego rodzaju konkurentów. Powoduje to, że więcej cząsteczek rozpuszczalnika przenika przez błonę w kierunku od roztworu mniej stężonego do bardziej stężonego, niż odwrotnie - zjawisko to nazywamy właśnie osmozą (czarna strzałka). Po pewnym czasie możemy zaobserwować zmianę objętości roztworów - w przypadku roztworu mniej stężonego zmniejszyła się (stężenie wzrosło), a u drugiego zwiększyła się (stężenie zmalało), co obrazuje Rys.1.B.
Plazmoliza jest wynikiem osmozy, w której rolę bariery półprzepuszczalnej pełnią błony biologiczne. W momencie zanurzenia komórki w bardziej stężonym w stosunku do jej wnętrza roztworze woda zaczyna wypływać przez błony biologiczne – np. błonę otaczającą wakuolę, czy błonę komórkową – na zewnątrz, co pociąga za sobą odwodnienie komórki i zmniejszenie się objętości protoplastu. Przeniesienie komórki, u której zaobserwowano już plazmolizę, do roztworu hipotonicznego spowoduje napływ wody do komórki i odzyskanie turgoru, co nazywamy deplazmolizą. Zarówno plazmoliza (poprzez odwodnienie komórki), jak i deplazmoliza (poprzez rozerwanie błon) mogą – choć nie muszą – prowadzić do śmierci komórki.
Literatura:
- [1] Kacperska A., Gospodarka wodna, w: Kopcewicz J., Lewak S., Fizjologia roślin, Wydawnictwo Naukowe PWN, Warszawa, 2002, str. 192-227 powrót
- [2] Szweykowska A., Fizjologia roślin, Wydawnictwo Naukowe Uniwersytetu im. Adama Mickiewicza w Poznaniu, Poznań, 1997, str. 41-59 powrót
- [3] Ples M., Niezwykłe bariery. O błonach półprzepuszczalnych i osmozie, Biologia w Szkole, 3 (2017), Forum Media Polska Sp. z o.o., str. 52-58 powrót
- [4] Ples M., Transport wody - jak to robią rośliny?, Biologia w Szkole, 5 (2017), Forum Media Polska Sp. z o.o., str. 59-638 powrót
- [5] Krześniak L. M., Apteczka Ziołowa, Wydawnictwo Sport i Turystyka, Warszawa, 1988 powrót
- [6] Onion History, w serwisie: https://www.onions-usa.org, dostępne online: https://www.onions-usa.org/all-about-onions/history-of-onions/ [dostęp 22.02.2020] powrót
- [7] Nowiński M., Dzieje upraw i roślin leczniczych, Państwowe Wydawnictwa Rolnicze i Leśne, Warszawa, 1983, str. 195 powrót
Autorem fotografii i rysunków jest Marek Ples.
Marek Ples