Kolorowy cylinder - błękit bromotymolowy i dwutlenek węgla
Poniższy artykuł został opublikowany pierwotnie w czasopiśmie dla nauczycieli Chemia w Szkole (4/2023):

Nauka przez doświadczenie od wieków była podstawową metodą poznawczą, dzięki której ludzkość zdobywała wiedzę o świecie. Obserwacje, próby, błędy i odkrycia stanowiły kluczowe elementy tego fascynującego procesu. W dzisiejszych czasach, gdzie nauka rozwija się w zastraszającym tempie, wciąż istnieje wyraźna potrzeba kładzenia nacisku na pozyskiwanie wiedzy w drodze doświadczeń. Pokazowe eksperymenty, zaprojektowane w celu demonstracji konkretnych zjawisk, mogą nie tylko zainteresować potencjalnych poszukiwaczy wiedzy, ale również ukazać głębsze prawidłowości tkwiące w badanych zjawiskach.
Wraz z postępem technologicznym i możliwościami zaawansowanych narzędzi naukowych, wiele badań przesunęło się w stronę skomplikowanych symulacji i eksperymentów, które są poza zasięgiem większości ludzi. Jednak pokazowe eksperymenty pozostają kluczowym narzędziem, pozwalającym na przekazanie wiedzy i wyjaśnienie złożonych zjawisk w zrozumiały sposób. Ich prostota, a zarazem efektowność, sprawia, że są one doskonałym narzędziem edukacyjnym, wzbudzającym zainteresowanie i ciekawość.
Nauka przez doświadczenie jest jednym z najbardziej wartościowych i naturalnych sposobów zdobywania wiedzy. Doświadczenia i eksperymenty (warto sobie uzmysłowić jakie różnice występują między tymi dwoma terminami) stanowią cenny element procesu edukacyjnego, umożliwiając zrozumienie skomplikowanych zjawisk w przystępny sposób. Kluczem do maksymalnego wykorzystania tego podejścia jest zdolność dostrzegania nie tylko samych efektów, ale także głębszych prawidłowości, które sprawiają, że nauka staje się fascynującą podróżą, w której możemy poznawać otaczający nas świat.

Prezentowane w tym artykule doświadczenie jest proste do przeprowadzenia, zapewnia niesamowity efekt wizualny, a jednocześnie w ciekawy sposób wprowadza w zagadnienia odczynu środowiska.
Czego potrzebujemy?
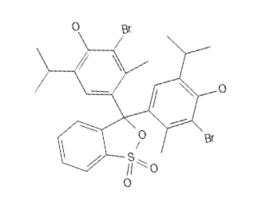
Potrzebujemy dibromotymolosulfoftaleiny C27H28Br2O5S (Rys.1). Związek ten jest inaczej nazywany błękitem bromotymolowym [1].
W warunkach normalnych ma on zwykle postać czerwono-pomarańczowego proszku (Fot.1), bardzo słabo nierozpuszczalnego w wodzie, natomiast całkiem dobrze w alkoholu etylowym C2H5OH. Alkoholowy roztwór tej substancji jest czerwony. W środowisku kwaśnym przybiera barwę żółtą, w zasadowym błękitną, a w środowisku obojętnym zieloną [2] [3].
Kolejną potrzebną substancją jest zestalony dwutlenek węgla CO2, czyli suchy lód. W zwykłych warunkach CO2 zestala się w temperaturze −78,5°C, a w temperaturze pokojowej nieustannie sublimuje.
Przydatny będzie także wodorotlenek sodu NaOH, w postaci stałej lub w rozcieńczonym roztworze.
Pamiętajmy, że błękit bromotymolowy jest toksyczny i rakotwórczy, a na skórze pozostawia trudne do usunięcia plamy. Zestalony dwutlenek węgla CO2 zachowuje bardzo niską temperaturę - należy zachować bezwzględną ostrożność! Dłuższy kontakt ze skórą może spowodować dotkliwe odmrożenia. Wodorotlenek sodu NaOH jest żrący.
Pokaz
Przygotowanie doświadczenia nie jest skomplikowane. Do cylindra miarowego, na przykład o pojemności 100cm3, należy wlać wodę destylowaną do około 3/4 objętości i bardzo delikatnie zalkalizować ją niewielkim dodatkiem wodorotlenku sodu - wystarczy kilka miligramów lub kilka kropli roztworu. Po dodaniu kilku kropli alkoholowego roztworu błękitu bromotymolowego ciecz przyjmuje barwę ciemnoniebieską (Fot.2).
Następnie do roztworu należy wrzucić niewielki fragment suchego lodu. Woda ma temperaturę równą około 20°C, jest więc o prawie sto stopni cieplejsza niż suchy lód! Nic więc dziwnego, że w kontakcie z nią ten ostatni intensywnie sublimuje. Niska temperatura powoduje skroplenie pary wodnej z powietrza, co objawia się powstaniem mgły.
Po chwili roztwór przyjmuje kolor zielony (Fot.3), a następnie żółty (Fot.4), co w połączeniu z odgłosem bulgotania, widocznymi pęcherzykami gazu i powstającą mgłą daje niesamowity efekt.
Niektórzy eksperymentatorzy mogą mieć problem ze zdobyciem suchego lodu. Mimo jego braku nie musimy jednak rezygnować z doświadczenia! Przez roztwór można przepuszczać strumień gazowego dwutlenku węgla CO2, co da ten sam efekt barwny (oczywiście oprócz powstania mgły). Skąd wziąć ten gaz? Możliwości jest wiele, ale doświadczenie możemy wykorzystać choćby do udowodnienia, że w wydychanym przez nas powietrzu jest obecna stosunkowo duża ilość tej substancji, ponieważ niebieski roztwór (bardzo delikatnie zalkalizowany, zbyt duża ilość zasady uniemożliwi obserwację efektu) widoczny na Fot.5, zmienia barwę podczas wdmuchiwania do niego powietrza z naszych płuc przy pomocy słomki (Fot.6).
Wyjaśnienie
Błękit bromotymolowy C27H28Br2O5S jest barwnikiem, chemicznym wskaźnikiem pH. Jego barwa zależy od odczynu środowiska, w którym się znajduje.
Roztwór użyty w doświadczeniu ma początkowo odczyn lekko zasadowy, co objawia się niebieskim zabarwieniem.
Podczas sublimacji CO2 jego część rozpuszcza się w wodzie. Powstają wtedy jony węglanowe CO32-, wodorowęglanowe HCO3- i oczywiście wodorowe H+. Z tego powodu pH roztworu obniża się, dzięki czemu wskaźnik przybiera najpierw barwę zieloną w środowisku obojętnym, a następnie żółtą w kwasowym.
W doświadczeniu można wykorzystać także inne wskaźniki kwasowo-zasadowe, uzyskując inne przejścia barwne.
Literatura:
- [1] Hassa R., Mrzigod J., Nowakowski J., Podręczny słownik chemiczny, Wyd. I, Videograf II, Katowice, 2004, str. 384 powrót
- [2] Lide D. R. (red.), CRC Handbook of Chemistry and Physics, wyd. 88, CRC Press, 2007, str. 8-16 powrót
- [3] De Meyer T., Substituent effects on absorption spectra of pH indicators: An experimental and computational study of sulfonphthaleine dyes, Dyes and Pigments, 2014, 102, str. 241-250 powrót
Wszystkie fotografie i rysunki zostały wykonane przez autora
Uzupełnienie autora
Efekt doświadczenia można zobaczyć na filmie:
Marek Ples





